隨著英國(United Kingdom, UK)自 2021 年 1 月 1 日起正式脫離歐盟(European Union, EU),醫療器材進入英國市場將採用嶄新的驗證模式與全新的產品驗證標誌 UKCA 或 CE UK(NI)。以下將從台灣製造商的角度出發,以深入淺出的方式剖析 UKCA 所帶來的衝擊和可能的影響。
1. 什麼是UKCA?
UKCA 為 UK Conformity Assessed 的縮寫,代表「英國符合性評鑑」。如同 CE 標誌,UKCA 也作為產品上的標誌。標示 UKCA 的產品將能夠進入大不列顛(Great Britain, GB)市場,這裡指的大不列顛市場只包含了英格蘭(England)、蘇格蘭(Scotland)和威爾斯(Wales),並不包含北愛爾蘭 (Northern Ireland)。值得注意的是,若產品只有單獨標示 UKCA,將無法進入北愛爾蘭市場。若產品打算進入北愛爾蘭市場,按照北愛爾蘭議定書 (Northern Ireland Protocol)的要求,需要有 CE 標誌或 CE UK(NI) 標誌,UK(NI) 標誌也可以稱為 UKNI 標誌。
2. 醫療器材要如何進入英國市場?
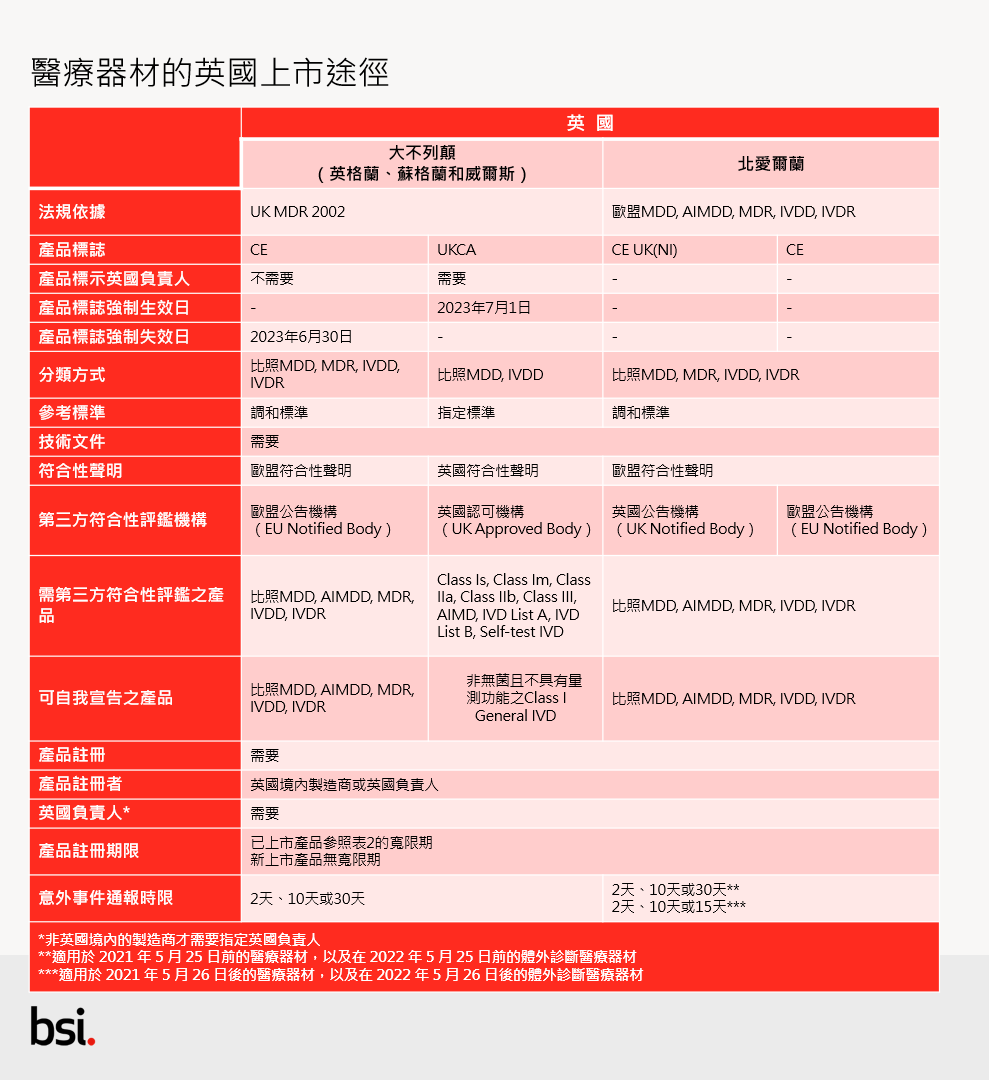
所有醫療器材都必須先向英國的藥物及保健產品管理局(Medicines & Healthcare products Regulatory Agency, MHRA)註冊後,才能夠進入英國市場。大部分的產品還必須先透過第三方機構完成符合性評鑑,取得相關證書後才能進行註冊。非英國境內的製造商應先指定唯一一名位在英國當地的負責人(UK Responsible Person),再由英國負責人向 MHRA 註冊製造商的醫療器材。醫療器材在英國的上市途徑可參考〈表 3〉。
在 2023 年 6 月 30 日緩衝期截止前,無論是有 CE 標誌或 UKCA 標誌的醫療器材,在 MHRA 註冊後,都可以進入大不列顛市場。有 CE 標誌的醫療器材若於 2021 年 1 月 1 日前就已經在英國市場流通,則必須在 MHRA 給予的寬限期(表 2)內完成醫療器材的註冊後,才能夠繼續進入英國市場。然而自 2023 年 7 月 1 日起,所有醫療器材都必須要有 UKCA 標誌,並在 MHRA 註冊後才能夠進入大不列顛市場。若產品打算進入北愛爾蘭市場,則需要有 CE 標誌或 CE UK(NI) 標誌。
3. 醫療器材在英國市場是依循哪一部法規?
由於大不列顛市場採用全新的 UKCA 模式,而北愛爾蘭市場則沿用歐盟的 CE 模式,大不列顛市場與北愛爾蘭市場有著截然不同的法規依據。
目前 UKCA 所依據的法規是「Medical Devices Regulations 2002 as amended by EU Exit Regulations of 2019 and 2020」,簡稱為 UK MDR 2002。UK MDR 2002 轉換並採納了歐盟MDD(93/42/EEC)、AIMDD(90/385/EEC)和 IVDD (98/79/EC)的法規要求,包含了醫療器材的分類方式與上市後監督(Post-market surveillance)模式,但不包含任何與 MDR(EU 2017/745)和 IVDR (EU 2017/746)有關的法規要求。其中 UK MDR 2002的第二編(Part II)可對應到MDD,第三編(Part III)可對應到 AIMDD,第四編(Part IV)可對應到 IVDD。英國正在制訂嶄新的醫療器材法規 Medicines and Medical Devices Act,作為未來醫療器材的法規基礎。
由於北愛爾蘭市場採用的是 CE 標誌或 CE UK(NI) 標誌,目前醫療器材在北愛爾蘭市場是依照歐盟的 MDD、AIMDD 和 IVDD 進行管理,並將隨著歐盟的 MDR 和 IVDR 分別從 2021 年 5 月 26 日和 2022 年 5 月 26 日開始生效而跟著實施 MDR 和 IVDR。
4. 什麼是UKCA標誌(UKCA mark)和CE UK(NI)標誌(CE UK(NI) mark)?
UKCA 標誌是一種專門用於大不列顛市場之產品標誌,UKCA 標誌無法用來進入歐盟、歐洲經濟區(European Economic Area, EEA)或北愛爾蘭市場。若產品打算進入北愛爾蘭市場,需要有 CE 標誌或 CE UK(NI) 標誌。
CE UK(NI) 標誌是一種專門用於北愛爾蘭市場之產品標誌,CE UK(NI) 標誌無法用來進入歐盟、歐洲經濟區或大不列顛市場。若產品打算進入大不列顛市場,需要有 UKCA 標誌,或者有CE標誌(僅適用於 2023 年 6 月 30 日緩衝期截止前)。若產品打算進入北愛爾蘭和歐盟市場,需要有 CE 標誌。
醫療器材在不同的市場需使用不同的產品標誌,如下〈表1〉所示。
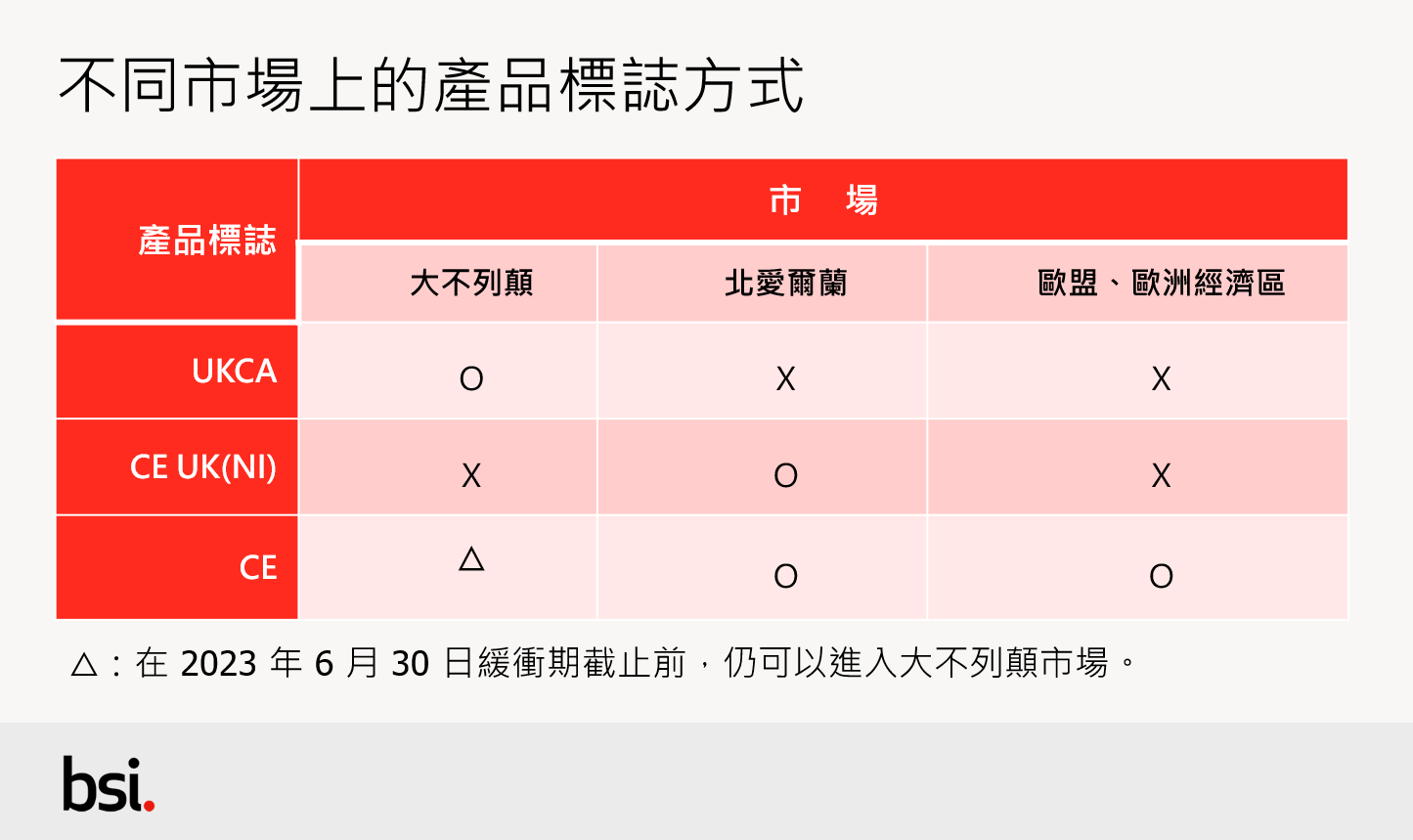
5. 何時開始必須使用UKCA標誌?
從 2021 年 1 月 1 日起至 2023 年 6 月 30 日止,符合 UKCA 相關要求的產品即可採用 UKCA 標誌。然而自 2023 年 7 月 1 日起,所有要進入大不列顛市場的醫療器材都必須要有 UKCA 標誌。
6. 如何標示UKCA和UK(NI) ?
如同 CE 標誌,依照醫療器材的分類與屬性,UKCA 和 UK(NI) 可以標示在產品上、包裝上或使用說明書上。UKCA 和 UK(NI) 標誌必須顯而易見、清晰且牢固,整體的 UKCA 和 UK(NI) 標誌至少要有 5 mm 高。標示時,應避免使用任何可能會對 UKCA 和 UK(NI) 產生誤解的標誌或記號,也不能在產品上放置任何可能會影響 UKCA 和 UK(NI) 標誌之能見度、辨識度或含意的其他標誌。當需要放大或縮小 UKCA 和 UK(NI) 標誌時,所有字母都必須依照〈圖 1〉和〈圖 2〉等比例縮放。

值得注意的是,UK(NI) 標誌絕不能單獨呈現,UK(NI) 標誌必須與 CE 標誌一併呈現。儘管 CE UK(NI) 這個標誌看起來包含了 CE 標誌,然而標示了 CE UK(NI) 的產品只能夠進入北愛爾蘭市場,既不能進入歐盟市場,也不能進入大不列顛市場。
另一方面,當英國境外的製造商在醫療器材的標籤或說明書上標示 UKCA 時,應呈現英國負責人(UK Responsible Person)的名稱和地址。不同於 CE 產品在標示授權代表的名稱和地址時,需使用特定的符號來識別授權代表,目前尚未有特定的符號用來識別英國負責人。此外只有 CE 標誌、但沒有 UKCA 或 UK(NI) 標誌的醫療器材於 2023 年 6 月 30 日緩衝期截止前要進入大不列顛市場時,儘管需要指定英國負責人來註冊醫療器材,但還不需要在標籤或說明書上註明英國負責人的名稱和地址。
若醫療器材需經由英國認可機構進行英國符合性評鑑,應將英國認可機構的代碼放置在 UKCA 標誌的下方。除非進口商或經銷商也同時擔任了英國負責人,目前進口商或經銷商的名稱和地址可以不用呈現在任何的標示上。客製化醫療器材、臨床試驗用醫療器材、性能評估(performance evaluation)用體外診斷醫療器材以及基於人道立場使用的不合規醫療器材,均不得標示 UKCA。臨床試驗用醫療器材應標示「exclusively for clinical investigation」。若醫療器材能同時滿足 CE 和 UKCA 的要求,產品上可以同時放置 CE 標誌和 UKCA 標誌。
7. 什麼情況下必須使用CE UK(NI) 標誌?
只有當下列三種情況同時出現時,製造商才需要考慮使用 CE UK(NI) 標誌。
- 產品只打算進入北愛爾蘭市場,而不打算進入歐盟市場。
- 產品必須透過第三方機構進行符合性評鑑。
- 製造商只考慮透過英國公告機構(UK Notified Body)進行 CE 符合性評鑑。
若產品打算進入北愛爾蘭和歐盟市場,製造商應在產品上使用 CE 標誌,如〈表 1〉所示。
8. 使用UKCA和UK(NI) 標誌是否還需要準備技術文件(technical documentation)和符合性聲明(declaration of conformity)?
無論醫療器材屬於何種分類,也不論醫療器材是否需透過第三方機構進行符合性評鑑,製造商都必須備妥技術文件,來證明醫療器材符合相關法令法規的要求。製造商也必須簽署符合性聲明,來聲明醫療器材符合相關法令法規的要求。製造商亦需保存技術文件和符合性聲明,以備相關主管機關查驗。欲進入大不列顛市場的製造商應簽署英國符合性聲明(UK declaration of conformity),並參考英國的指定標準(designated standard)。欲進入北愛爾蘭市場的製造商則應簽署歐盟符合性聲明(EU declaration of conformity),並參考歐盟的調和標準(harmonized standard)。
指定標準涵蓋了BS、EN、EN ISO與EN IEC這四種字母開頭的標準,由於目前BSI仍是歐洲標準委員會(European Committee for Standardization, CEN)與歐洲電子技術標準委員會(European Committee for Electrotechnical Standardization, CENELEC)的成員,EN、EN ISO與EN IEC這三種字母開頭的標準仍可作為指定標準。英國的衛生與社會關懷部(Department of Health and Social Care)已於2021年1月6日公告了276份指定標準供製造商參考,目前這276份指定標準皆屬於歐盟標準(EN standard)。
9. 什麼情況下必須透過第三方機構進行符合性評鑑?
大不列顛市場與北愛爾蘭市場有著截然不同的第三方符合性評鑑模式。大不列顛市場採用全新的英國符合性評鑑,北愛爾蘭市場則沿用歐盟的CE符合性評鑑,如〈表 3〉所示。
由於目前UK MDR 2002仍採納了歐盟MDD和IVDD的分類方式,只有MDD範圍下不屬於無菌、也不具有量測功能的Class I醫療器材,或者屬於IVDD範圍下但未列在清單A(List A)和清單B(List B)上、亦不用於自我檢測(self-testing)的一般(General)醫療器材可免除經由英國認可機構(UK Approved Body)來進行英國符合性評鑑。其他種類的醫療器材(Class Is, Class Im, Class IIa, Class IIb, Class III, AIMD, IVD List A, IVD List B, Self-test IVD) 都必須透過英國認可機構完成英國符合性評鑑後,才可以進行UKCA標誌。
若醫療器材打算進入北愛爾蘭市場,且屬於Class Is, Class Im, Class IIa, Class IIb, Class III, AIMD, IVD List A, IVD List B, Self-test IVD其中的任何一類,則必須先透過歐盟公告機構(EU Notified Body)完成CE符合性評鑑後,才可以進行CE標誌,或者透過英國公告機構(UK Notified Body)完成CE符合性評鑑後,再進行CE UK(NI) 標誌。
10. 可以進行英國符合性評鑑的英國認可機構有哪些?
目前已具備英國符合性評鑑資格的英國認可機構共計有三間*,BSI Assurance UK Ltd(代碼0086)是其中一間,並且是唯一具備醫療器材、主動式植入醫療器材和體外診斷醫療器材完整資格的英國認可機構。
*最新名單詳見:UK approved bodies listed under Medical Devices Regulations 2002
11. 能否採用自我宣告(self-declaration)的方式進行UKCA標誌?
如同歐盟的 MDD 和 IVDD,部分醫療器材可以採用自我宣告的方式進行 UKCA 標誌。由於目前 UK MDR 2002 仍採納了歐盟 MDD 和 IVDD 的分類方式,若醫療器材屬於 MDD 範圍下不屬於無菌、也不具有量測功能的 Class I 醫療器材,或者屬於 IVDD 範圍下但未列在清單 A(List A)和清單 B(List B)上、亦不用於自我檢測(self-testing)的一般(General)醫療器材,則可以採用自我宣告的方式進行 UKCA 標誌。
12. 只有CE標誌的醫療器材能否進入英國市場?
由於英國市場分為大不列顛市場和北愛爾蘭市場,醫療器材在這兩個市場的上市模式需分開看待,如〈表 3〉所示。
只有 CE 標誌、但沒有 UKCA 標誌的醫療器材,在 2023 年 6 月 30 日緩衝期截止前,仍可以進入大不列顛市場。這裡指的 CE 標誌包含了任何依照歐盟 MDD(93/42/EEC)、AIMDD(90/385/EEC)、MDR(EU 2017/745)、IVDD(98/79/EC)或 IVDR(EU 2017/746)的要求,所進行的 CE 標誌。然而自 2023 年 7 月 1 日起,只有 CE 標誌、但沒有 UKCA 標誌的醫療器材,將無法進入大不列顛市場。
反之只有 CE 標誌、但沒有 UKCA 或 UK(NI) 標誌的醫療器材,無論是在 2023 年 6 月 30 日緩衝期截止前或截止後,都可以持續在北愛爾蘭市場流通。
13. 何時開始必須向MHRA註冊醫療器材?
自 2021 年 1 月 1 日起,無論醫療器材是否有 CE 標誌或 UKCA 標誌,所有醫療器材都必須先向 MHRA 註冊後,才能夠進入英國市場。針對目前已在市場上流通的醫療器材,MHRA 也給予了製造商一些寬限期來註冊醫療器材,寬限期依照醫療器材的風險等級有所不同,如下〈表 2〉所示。

客製化(custom-made)醫療器材的強制註冊生效日依照其所屬的醫療器材類別實施。需留意的是,在 2021 年 1 月 1 日前即著手註冊的 Class I 醫療器材和一般用體外診斷醫療器材(IVD),不適用上述的寬限期,仍需繼續完成註冊程序。
14. 誰必須向MHRA註冊醫療器材?
英國境內的製造商可以直接向MHRA註冊醫療器材,而非英國境內的製造商應先指定唯一一名位在英國當地的負責人(UK Responsible Person),再由英國負責人向 MHRA 註冊製造商的醫療器材。英國境外的製造商應盡速指定英國的負責人,方能在寬限期內完成註冊程序。
15. 誰可以擔任英國負責人(UK Responsible Person)?
目前任何在英國(包含了英格蘭、蘇格蘭、威爾斯和北愛爾蘭)當地有營業登記的法人,都可以擔任英國負責人。進口商和經銷商都不需要指定英國負責人,但可以擔任英國負責人。
16. 英國負責人(UK Responsible Person)有哪些職責?
英國負責人代表非英國境內的製造商,履行下列職責。
- 向 MHRA 註冊製造商的醫療器材。
- 確保製造商已制定符合性聲明(declaration of conformity)與技術文件(technical documentation)。若醫療器材需經過符合性評鑑程序 (conformity assessment procedure),亦需確保製造商已完成適當的符合性評鑑程序。
- 保存符合性聲明與技術文件之副本供 MHRA 檢查。若醫療器材有相關證書,亦需保存相關證書之副本。
- 當 MHRA 有要求時,提供 MHRA 所有必要的資訊與文件,來證明醫療器材之符合性。
- 當 MHRA 有要求時,提供 MHRA 醫療器材之樣品,或提供 MHRA 能夠取得醫療器材樣品之管道。
- 倘若英國負責人無法提供醫療器材之樣品,也無法提供能夠取得醫療器材樣品之管道,當 MHRA 有要求時,需負責聯繫製造商以傳達 MHRA 的要求,並將製造商是否願意提供樣品的意願傳達給 MHRA。
- 與 MHRA 合作採取矯正或預防措施,以消除或減緩醫療器材所造成的風險。
- 立即通知製造商與受託醫療器材有關的抱怨,以及從健康照護專業人員、病患和使用者通報的可疑事件。
- 若製造商違反法規上的義務,中止與製造商之間的法律關係,並通知 MHRA。必要時,亦需通知英國認可機構(UK Approved Body)。
17. UKCA和CE UK(NI) 採用何種上市後監督(Post-market surveillance)模式?
由於大不列顛市場採用的是 UKCA 標誌,而 UKCA 所依據的法規 UK MDR 2002 並不會隨著 MDR 和 IVDR 的生效而改變,醫療器材(即 MDD 和 AIMD 範疇下的醫療器材)與體外診斷醫療器材(即 IVDD 範疇下的體外診斷醫療器材)仍將繼續維持目前意外事件的通報時限,並依照意外事件的嚴重程度分為 2 天、10 天或 30 天。
由於北愛爾蘭市場採用的是 CE 標誌或 CE UK(NI) 標誌,隨著歐盟的 MDR 和 IVDR 將分別自 2021 年 5 月 26 日和 2022 年 5 月 26 日起在北愛爾蘭市場開始生效,醫療器材(即MDD、AIMD 和 MDR 範疇下的醫療器材)與體外診斷醫療器材(即 IVDD 和 IVDR 範疇下的體外診斷醫療器材)的意外事件通報時限也將分別自 2021 年 5 月 26 日和 2022 年 5 月 26 日起,依照意外事件的嚴重程度調整為 2 天、10 天或 30 天。

BSI 客戶經理 蔡騰寬(Jeff Tsai)撰文
2021 年 4 月


